Une filière porcine en pleine mutation
Depuis quelques décennies déjà, l’élevage porcin fait face à des enjeux de taille en s’engageant dans une démarche d’amélioration continue du bien-être animal, de la sécurité alimentaire, de son image auprès des consommateurs et de son impact environnemental1.
3e pays européen producteur de viande de porc, avec 2,1 millions de tonnes produites en 2023, la filière porcine française demeure un secteur porteur et économique2. De plus, la viande de porc représente encore 38% de la consommation de viande, ce qui en fait la viande la plus consommée dans le monde.
Cependant, la filière porcine est menacée par l’émergence permanente de nouvelles maladies, pouvant devenir préoccupantes. Il est devenu nécessaire pour les opérateurs de la filière porcine de disposer d’un protocole, permettant la conservation des races en cas d’apparition de foyers épidémiques, dans la faune sauvage ou dans les élevages de production.
Projet Cryopig, quelles voies pour la filière porcine ?
La finalité du projet Cryopig, initié en 2020, en partenariat avec l’école VetAgroSup, l’ISARA de Lyon et l’IFIP, est à la fois de créer de nouvelles connaissances scientifiques dans le domaine des biotechnologies de la reproduction chez le porc, mais aussi de proposer des solutions industrialisables, répondant aux défis auxquels fait face aujourd’hui la filière porcine.
L’étude de ce domaine encore novateur est un axe de développement stratégique et à long terme pour le Groupe Axiom. L’une des motivations concerne la sauvegarde des races porcines pour une préservation du patrimoine et de la diversité génétique du cheptel. A plus long terme, il est possible d’imaginer un nouvel outil de diffusion génétique.
Celui-ci pourrait pallier les diverses problématiques liées au transport d’animaux vivants en se concentrant uniquement sur le maintien d’une température optimale lors du transport des embryons.
A plus long terme, il serait possible d’envisager la création de centres de « réponse » pour accélérer la réimplantation d’une race, ou la reconstitution d’un cheptel entier après sa disparition, à cause d’une épidémie particulièrement virulente, comme cela a été le cas en Chine avec la PPA (Peste Porcine Africaine) en 2018.
La Cryobanque nationale, rôle de contributrice à la sauvegarde de la variabilité génétique
C’est dans ce contexte qu’une banque cryogénique de semences porcine a été mise en place il y a plusieurs années au sein de la Cryobanque Nationale (Cf. CRB-Anim). Mais la reconstitution d’une race en danger ou d’une lignée génétique spécifique nécessite de pouvoir disposer d’embryons ou d’ovocytes cryoconservés. Une telle cryobanque permet également une gestion de la diversité génétique porcine, une utilisation à long terme de ces ressources, et en particulier, la sauvegarde des races locales à faible effectifs, dont la situation reste critique face aux risques sanitaires actuels.
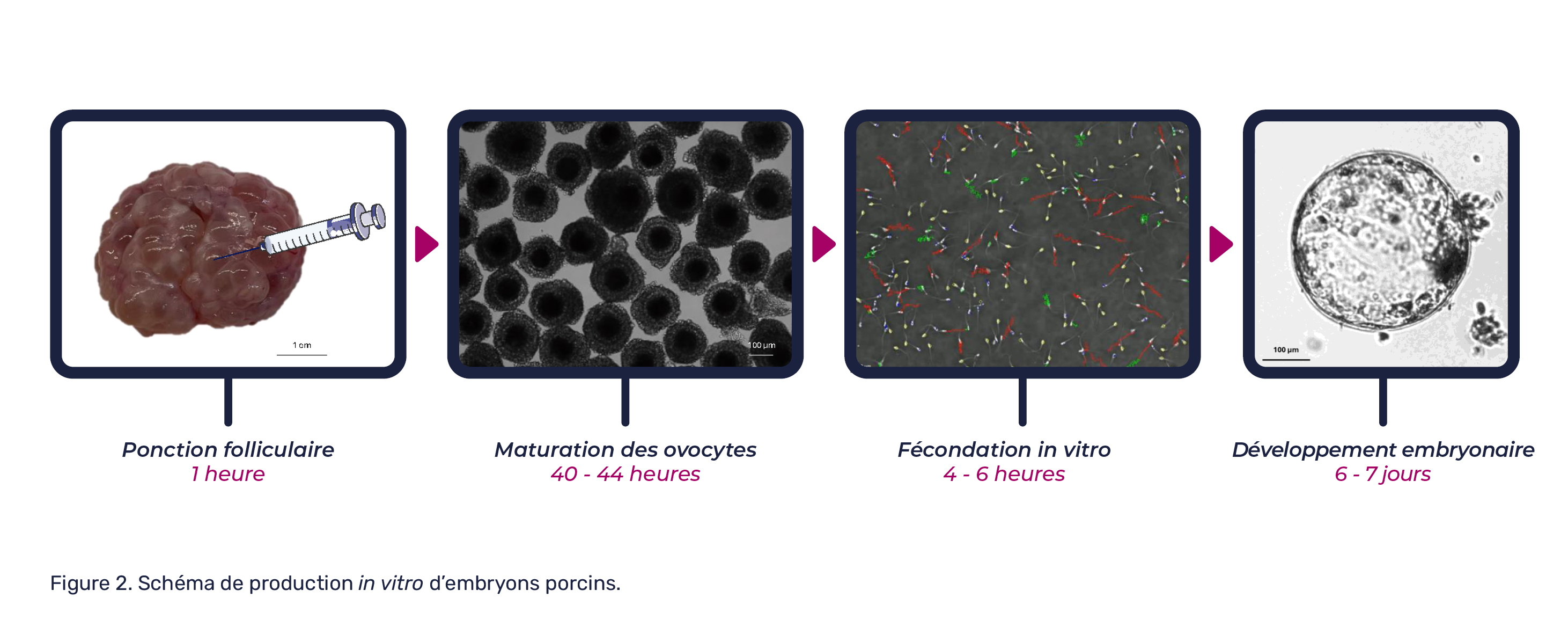
Passons désormais à l’aspect scientifique de cette méthode, en explorant les recherches menées par nos équipes sur les étapes de la production in vitro des embryons porcins.
Bien que les premiers succès de production in vitro d’embryons chez le porc remontent à 1986, le taux de réussite reste relativement variable. Les principaux défis rencontrés dans l’espèce porcine sont l’incidence élevée de la polyspermie*, le blocage des embryons au stade quatre-cellules (stade associé à l’activation du génome embryonnaire chez les mammifères) et les faibles taux de blastocystes3.
La maîtrise et la transformation de la composition des milieux de culture (maturation, fécondation et développement) sont un facteur clé pour lever ces verrous. Il a été montré que la survie, post-décongélation, des embryons dépendait fortement des systèmes de cultures5. Enfin, le bon développement in vivo d’un individu repose sur la mise en place correcte de ses premières lignées cellulaires puisque ce sont ces dernières qui permettront l’implantation8 et le développement foetal.
« L’objectif scientifique de ce projet est de caractériser les effets et d’étudier les interactions des facteurs qui compromettent aujourd’hui la production in vitro d’embryons porcins et leur cryoconservation ; le but étant à terme, de conserver des embryons »
Cryopig, quelles grandes étapes comme ligne directrice d’un protocole favorisant le taux d’embryons transférés, avec succès, après cryoconservation ?
Le projet de thèse est organisé en « cascade », les connaissances acquises à chacune des différentes étapes de la production in vitro (maturation, fécondation, développement) et de la cryoconservation des embryons porcins, permettant de passer à la suivante.

1ère étape : Quels sont les facteurs impactant le développement des embryons produits in vitro ?
La littérature actuelle montre qu’il n’existe pour le moment pas de protocole universel de production in vitro chez le porc, en raison notamment d’une absence de milieux chimiquement définis, de l’utilisation de produits naturels et du rôle incertain de nombreux additifs dans ces milieux3. De fait, les taux d’embryons produits in vitro sont relativement faibles dans la grande majorité des expérimentations. Parallèlement, le stade et la qualité embryonnaire restent majoritairement non déterminés.
L’objectif de cette première étape est donc d’identifier l’ensemble des facteurs à même d’impacter le développement de ces embryons, jusqu’au stade embryonnaire souhaité. L’une des voies envisagées porte sur l’adaptation des milieux de culture. Ainsi, l’embryon pourrait bénéficier d’un apport de différents additifs lors des différentes étapes de son développement via l’utilisation de milieux séquentiels. Ainsi, à l’inverse d’un unique milieu pour l’ensemble de son développement in vitro, il s’agirait de varier, au cours du temps, la composition des milieux pour mieux imiter les besoins de l’embryon in vivo, en fonction de son stade de développement.
En effet, l’embryon ne nécessitant pas les mêmes apports tout au long de son développement, l’ajout ou le retrait de certaines molécules à des étapes clés pourraient avoir un effet bénéfique sur la formation de blastocystes*.
2ème étape : Quelles sont les conditions optimales pour la bonne cryoconservation des embryons produits in vitro ?
Les protocoles de cryoconservation s’appuient sur l’utilisation de solutions, protégeant l’embryon des effets néfastes des phénomènes physiques de la congélation, dont la nature et la concentration varient considérablement selon les systèmes étudiés.
Les durées d’incubation dans ces solutions, tout comme les méthodes existantes de refroidissement et de réchauffement adaptées (congélation lente, vitrification) peuvent également impacter la survie des embryons.
L’objectif de cette étape est d’identifier les effets de chacun de ces paramètres sur la survie des embryons produits in vitro (morulas ou blastocystes) ainsi que leurs interactions, afin d’établir un protocole de cryoconservation adapté aux embryons porcins. Pour cela, la toxicité des solutions cryoprotectrices sera évaluée sur des embryons produits in vitro, sans application des étapes de refroidissement et de réchauffement. Ainsi, cette étape nous permettra d’établir une liste de solutions dénuées d’impacts néfastes (ou négligeables) pour le maintien de l’embryon après son refroidissement et avant son réchauffement.
3ème étape : L’impact des différents facteurs précédemment étudiés sur les conditions de transfert des embryons produits in vitro puis cryoconservés
Après avoir identifié les conditions optimales de cryoconservation des embryons porcins produits in vitro, le but de la troisième étape est d’identifier les marqueurs caractéristiques du potentiel de développement des embryons et donc de leur qualité.
L’évaluation de l’expression de gènes de pluripotence (tels que Oct4, Nanog, Sox2, Cdx2)4 sera réalisée afin d’observer la mise en place des premiers feuillets embryonnaires (masse cellulaire interne et trophectoderme) nécessaires au développement in vivo d’un nouvel individu8. L’expression de ces gènes est prépondérante pour la mise en place du plan d’organisation de l’organisme, essentiel aux prémices de la gestation.
L’anatomie particulière de l’appareil génital de la truie a rendu difficile la mise au point de procédures de transfert simples et non invasives, ou du moins minimales. Au cours de la dernière décennie, de nouvelles procédures ont été mises au point, qui permettent des transferts embryonnaires non-chirurgicaux tout en préservant efficacement les embryons. L’absence de chirurgie et la préservation des embryons à ce stade sont essentielles pour répondre aux attentes sociétales liées au bien-être animal6. Ainsi, les protocoles de cryoconservation qui auront permis d’obtenir les meilleurs résultats, seront retenus pour la production et la cryoconservation des embryons porcins.
Dans le cadre du projet Cryopig, la méthode de transfert envisagée sera une méthode non-chirurgicale, avec un site de dépôt intra-utérin profond6. Un suivi de gestation sera réalisé afin de confirmer l’implantation et le développement des embryons. En effet, pour les truies gestantes parvenues à terme, les taux de survie à la mise bas seront calculés et un suivi longitudinal (examens échographiques hebdomadaires, profils hormonaux) au cours des 115 jours de gestation permettra de confirmer qu’il n’y a pas d’avortement.
Conclusion
De manière générale, le développement de cette technologie et la création de protocoles efficaces à toutes ses étapes permet d’entrevoir de multiples possibilités, et de développer un nouvel outil de diffusion génétique, qui révolutionnera le transport et la filière porcine dans son ensemble.
Rédacteur(s)
- Article rédigé par Victoria Slezec-Frick, Doctorante chez Axiom et VetAgroSup.
- Article vulgarisé par le service Communication d’Axiom
Quelques aides pour une meilleure compréhension de l’article
- Cryobanque : Banque (ici de semences et d’embryons) de conservation par cryogénie, à des fins de préservation des espèces.
- Ovocyte : Terme scientifique de l’ovule.
- In vitro : Se dit des réactions chimiques, physiques, immunologiques ou de toutes les expériences et recherches pratiquées au laboratoire, en dehors d’un organisme vivant.
- Polyspermie : Pénétration d’un ovule de par plus d’un spermatozoïde. Ce phénomène peut engendrer des problèmes de développement ultérieurs. C’est l’opposé de la monospermie qui est le phénomène naturel normal, soit la pénétration d’un ovocyte par un seul spermatozoïde.
- Blastocyste : Stade très précoce de l’embryon, postérieur au stade morula, dénommé blastocyste dès que celui-ci présente un début de cavité en son centre. Ce stade est généralement le dernier stade observable in vitro. Le blastocyste est observable microscopiquement chez le porc, à partir du 5ème jour après fécondation.
- Morula : Stade très précoce de l’embryon, dénommé morula dès que celui-ci dénombre 16 à 32 cellules tout en présentant une absence de cavité en son centre. La morula est observable microscopiquement chez le porc, à partir du 4ème jour après fécondation.
- Trophectoderme : Nom donné à certaines cellules du blastocyste lors du développement embryonnaire précoce. Ces cellules permettent l’implantation de l’embryon dans l’endomètre maternel. Il est également à l’origine des annexes embryonnaires comme le placenta.
- Masse cellulaire interne : Nom donné à certaines cellules du blastocyste lors du développement embryonnaire précoce. Certaines de ses cellules sont à l’origine du développement du fœtus.
Sources et Bibliographies
- Bidanel, J.-P., et al., 2020. Cinquante années d’amélioration génétique du porc en France : bilan et perspectives. INRAE Prod. Anim., 33. https://doi.org/10.20870/productions-animales.2020.33.1.3092
- Eurostat et douanes. https://lekiosque.finances.gouv.fr/Default.asp
- Fowler, K.E., et al., 2018. The production of pig preimplantation embryos in vitro: Current progress and future prospects. Reprod. Biol., 18, 203–211. https://doi.org/10.1016/j.repbio.2018.07.001
- Hall, V.J., 2013. Early development of the porcine embryo: the importance of cell signalling in development of pluripotent cell lines. Reprod. Fertil. Dev., 25, 94. https://doi.org/10.1071/RD12264
- Lowe, J.L., et al., 2017. Supplementation of culture medium with L-carnitine improves the development and cryotolerance of in vitro-produced porcine embryos. Reprod. Fertil. Dev., 29, 2357. https://doi.org/10.1071/RD16442
- Martinez, E.A., et al., 2019. Achievements and future perspectives of embryo transfer technology in pigs. Reprod. Domest. Anim., 54, 4–13. https://doi.org/10.1111/rda.13465
- Mucci, N., et al., 2006. Effect of estrous cow serum during bovine embryo culture on blastocyst development and cryotolerance after slow freezing or vitrification. Theriogenology, 65, 1551–1562. https://doi.org/10.1016/j.theriogenology.2005.08.020
- Surani, M.A., Barton, S.C., 1977. Trophoblastic vesicles of preimplantation blastocysts can enter into quiescence in the absence of inner cell mass. J. Embryol. Exp. Morphol., 39, 273–277. https://doi.org/10.1242/dev.39.1.273
